Halogen Dalam Kehidupan Sehari-hari
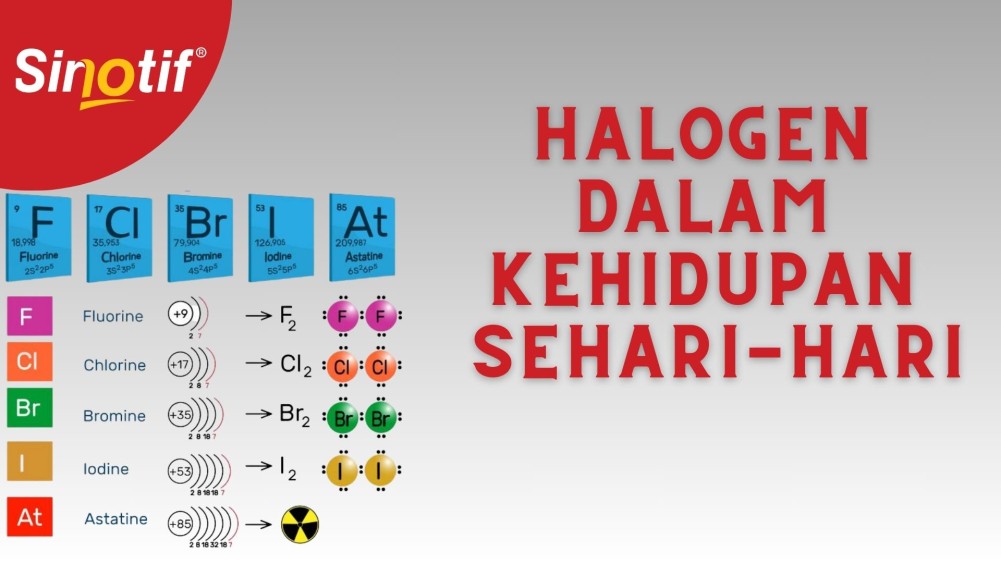
Halogen adalah unsur non logam yang terletak pada golongan VIIA pada sistem periodik unsur. Halogen berasal dari kata halos = garam, genes = pembentuk maka dari itu halogen disebut pembentuk garam. Halogen sangat reaktif dan mudah untuk menerima 1e pada elektron terluarnya sehingga cenderung membentuk ion negatif bermuatan negatif satu. Unsur halogen dapat membentuk molekul diatomik. Unsur halogen terdiri dari Fluor (F), Klorin (Cl), Bromin (Br), Iodin (I), dan Astatin (At). Unsur tersebut memiliki 7 elektron valensi pada subkulit ns2 np5.
Kelimpahan Unsur Halogen di Alam
|
Unsur |
Kelimpahan di Alam |
|---|---|
|
Flourin |
fluorit (CaF2) atau sianida fluorspar (CaF2) |
|
Klorin |
Garam NaCl, KCl, MgCl2 |
|
Bromin |
Terdapat pada logam bromide pada air di laut mati |
|
Iodin |
NaIO3 (natrium iodat) |
|
Astatin |
Jumlah nya sangat sedikit karena bersifat radioaktif |
Sifat Fisik Unsur Halogen
Sifat halogen yang dapat dikenali adalah bau yang menusuk. Kelima unsur halogen ini juga memiliki warna dan bentuk yang berbeda-beda. Fluorin adalah gas warna hijau pucat, klorin gas kuning kehijauan, bromin berbentuk cairan berwarna coklat kemerahan, iodin adalah benda padat abu-abu yang menyublim menjadi uap warna ungu. Dan astatin adalah benda padat dan mengandung daya radioaktif.
Perbedaan wujud unsur halogen mempengaruhi titik didih dan titik lelehnya. Semakin padat semakin besar titik didih dan titik lelehnya. Berikut ini tabel secara lengkap sifat fisik halogen :
Sifat Kimia Unsur Halogen
Halogen merupakan unsur yang sangat reaktif.Halogen merupakan oksidator kuat. Oleh karena itu mudah mengikat elektron atau mudah tereduksi. Urutan kekuatan oksidator golongan halogen: F2 > Cl2 > Br2 > I2 . Mempunyai bilangan oksidasi lebih dari satu, kecuali flour. Semua unsur halogen dapat bereaksi dengan gas hidrogen membentuk hidrogen halida. Kelarutan flourin, klorin, dan bromin dalam air mudah larut. Iodin sukar larut dalam air namun mudah larut dalam larutan KI. Halogen dapat menjadi racun jika diterima dalam jumlah yang cukup besar. Oleh karena itu, halogen harus digunakan dengan hati-hati dan dalam jumlah yang sesuai dengan tujuan yang diinginkan.
Manfaat Halogen Dalam Kehidupan Sehari-hari
1. Fluorin
-
CFC (Freon) digunakan sebagai cairan pendingin pada mesin pendingin, seperti AC dan kulkas. Freon juga digunakan sebagai propelena aerosol pada bahan-bahan semprot. Penggunaan Freon dapat merusak lapisan ozon.
-
Teflon (polietrafluoroetilena). Monomernya CF2 = CF2, yaitu sejenis plastik yang tahan panas dan anti lengket serta tahan bahan kimia, digunakan untuk melapisi panci atau alat rumah tangga yang tahan panas dan anti lengket.
-
Garam fluoride ditambahkan pada pasta gigi atau air minum untuk mencegah kerusakan gigi.
2. Klorin
-
Senyawa natrium hipoklorit (NaClO) dapat digunakan sebagai zat pemutih pada pakaian.
-
Senyawa natrium hipoklorit (NaClO) dapat digunakan sebagai zat pemutih pada pakaian.
-
Polivinil klorida (PVC) untuk membuat paralon.
-
Dikloro difenil trikloroetana (DDT) untuk insektisida.
-
Kloroform (CHCl3) untuk obat bius dan pelarut.
3. Bromin
-
Etil bromida (C2H4Br2) suatu zat aditif yang dicampurkan kedalam bensin bertimbal (TEL) untuk mengikat timbal, sehingga tidak melekat pada silinder atau piston. Timbal tersebut akan membentuk PbBr2 yang mudah menguap dan keluar bersama-sama dengan gas buangan dan akan mencemarkan udara.
-
AgBr merupakan bahan yang sensitif terhadap cahaya dan digunakan dalam film fotografi.
-
Natrium bromide (NaBr) sebagai obat penenang saraf
4. Iodin
-
Iodin Banyak digunakan untuk obat luka (larutan iodin dalam alkohol yang dikenal dengan iodium tingtur)
-
KI digunakan sebagai obat anti jamur.
-
Iodoform (CHI3) digunakan sebagai zat antiseptik.
-
AgI digunakan bersama-sama dengan AgBr dalam film fotografi.
-
NaI dan NaIO3 atau KIO3 dicampur dengan NaCl untuk mencegah penyakit gondok. Kekurangan iodium pada wanita hamil akan mempengaruhi tingkat kecerdasan pada bayi yang dikandungnya.